Monika Humaj ![]() 1*, Jerzy Mikosz
1*, Jerzy Mikosz ![]() 2, Gian Francesco Meloni
2, Gian Francesco Meloni ![]() 3
3
Afiliacje
1 Politechnika Krakowska im. Tadeusza Kościuszki, Szkoła Doktorska PK, Wydział Inżynierii Środowiska i Energetyki
2 Politechnika Krakowska, Wydział Inżynierii Środowiska i Energetyki, Katedra Technologii Środowiskowych
3 University of Cagliari, Faculty of Engineering and Architecture, Department of Environmental Engineering
*Kontakt / Correspondence: monika.humaj@doktorant.pk.edu.pl
DOI: 10.65545/GWITS.2026.01.05, GWiTS 1/2026, styczeń 2026
Pobierz PDF (Open Access)
Streszczenie:
W artykule przedstawiono historię rozwoju mikrobiologicznych ogniw paliwowych od ich powstania do czasów współczesnych. Wskazano na najważniejsze ograniczenia w zastosowaniu, które związane były z niskim natężeniem prądu i niestabilnością układów. Omówiono rozwój technologii oparty na doborze mikroorganizmów, wzbogacaniu substratu oraz optymalizacji materiałowej anod, membran i katalizatorów. Opisano również współczesne zastosowania MFC w roli biosensorów oraz źródeł zasilania dla urządzeń rozproszonych. Podano także przykłady wdrożeń pilotażowych MFC w oczyszczalniach ścieków i przedstawiono główne wyzwania, które na obecnym etapie rozwoju stanowią barierę dla powszechnego wykorzystania tego rozwiązania w skali przemysłowej.
Słowa kluczowe: ogniwa paliwowe, biosensory, wdrożenia pilotażowe MFC
Abstract:
The article presents the history of the development of microbial fuel cells from their inception to the present day. It highlights the most significant limitations in their application, which were related to low current density and system instability. It discusses the development of technology based on the selection of microorganisms, substrate enrichment and material optimisation of anodes, membranes and catalysts. It also describes contemporary applications of MFCs as biosensors and power sources for distributed devices. Examples of MFC pilot implementations in sewage treatment plants are given and the main challenges that currently constitute a barrier to the widespread use of this solution on an industrial scale are presented.
Keywords: fuel cells, biosensors, MFC pilot implementations
1. Wprowadzenie
Mikrobiologiczne ogniwo paliwowe (rys. 1) jest urządzeniem, w którym energia elektryczna wytwarzana jest w procesie utleniania materii organicznej przez mikroorganizmy. Proces ten opiera się na potencjale redoks pomiędzy donorem i akceptorem elektronów, jednak, w przeciwieństwie do chemicznych ogniw paliwowych, zamiast bezpośredniej reakcji wodoru i tlenu, energię dostarczają żywe komórki bakteryjne [9].
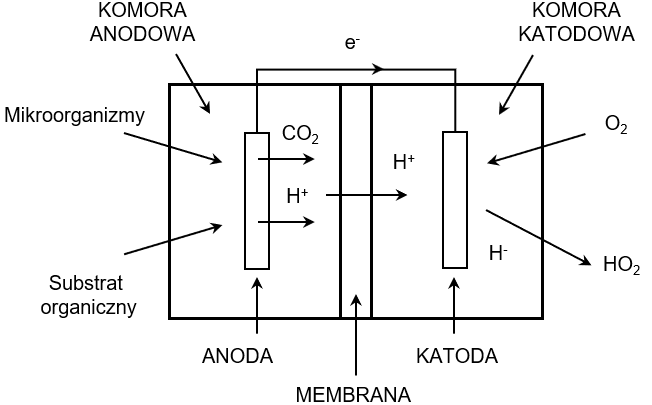
Fig. 1. MFC operation diagram, own work
Choć istnieje wiele różnych konfiguracji, standardowy system MFC zbudowany jest z katody i anody, które oddzielone są od siebie za pomocą membrany półprzepuszczalnej. W komorze anodowej, utrzymywanej w warunkach beztlenowych, znajduje się anoda (wykonana zazwyczaj z materiałów węglowych) oraz biofilm złożony z mikroorganizmów. Bakterie metabolizują materię organiczną, w wyniku czego dochodzi do rozerwania wiązań chemicznych i uwolnienia elektronów oraz protonów H+. Poprzez bezpośredni kontakt między białkami błonowymi a materiałem anody (zewnątrzkomórkowy transfer elektronów, EET) dochodzi do przeniesienia elektronów z wnętrza komórki na powierzchnię anody. Równocześnie protony uwalniane są do elektrolitu, a następnie przemieszczają się do komory katodowej. Transport ten odbywa się poprzez membranę, która przepuszcza protony i jednocześnie blokuje transport elektronów. Przepływ protonów przez membranę napędzany jest różnicą stężeń oraz różnicą potencjałów elektrochemicznych między komorami. Jako, że elektrony powstałe na anodzie nie mogą bezpośrednio przepłynąć przez membranę, skierowane zostają na obwód zewnętrzny. Tam dochodzi do utworzenia się różnicy potencjałów, co przekłada się na powstanie napięcia elektrycznego. Następnie elektrony, które przepłynęły przez obwód zewnętrzny, docierają do katody, gdzie łączą się z akceptorem elektronów (w większości MFC jest to tlen). Wytwarzany jest w ten sposób produkt uboczny procesu, czyli woda. Katoda jest zazwyczaj wykonana z materiału węglowego, pokrytego katalizatorem, który ułatwia redukcję tlenu [9].
2. Początki rozwoju koncepcji MFC
Za początki mikrobiologicznych ogniw paliwowych uważa się odkrycie Pottera, który w 1911 r. udowodnił występowanie zjawiska wytwarzania energii elektrycznej wskutek rozkładu substratów organicznych przez mikroorganizmy [25]. W trakcie doświadczeń przeprowadzonych na drożdżach Saccharomyces cerevisiae podczas fermentacji cukrów, wygenerowane zostało napięcie elektryczne wynoszące 0,3 – 0,5 V. Potter podobne zjawisko zaobserwował także dla bakterii Escherichia coli. Skalowalność tego rozwiązania zbadał w 1931 r. Cohen [12]. Przeprowadzone przez niego doświadczenie opierało się na szeregowym połączeniu wielu miniaturowych półogniw o objętości 10 ml z fermentującymi bakteriami. Choć utworzony w ten sposób układ wygenerował 35 V napięcia, uzyskano bardzo małe natężenie, rzędu 2 mA. Cohen wykazał tym samym, że zwiększanie liczby ogniw pozwala podnieść napięcie, lecz istnieje problem minimalnego natężenia prądu, a także złożoności takiego układu.
W latach 60. XX wieku rozwojem układów elektrochemicznych zaczęła interesować się amerykańska agencja lotów kosmicznych NASA. Przy planowaniu misji załogowych rozważano możliwość wykorzystania mikroorganizmów do jednoczesnego utylizowania odpadów organicznych oraz produkcji energii. W wyniku przeprowadzonych badań wykazano, że mikrobiologiczne przetwarzanie moczu przez bakterie Bacillus pasteurii bezpośrednio wpływało na zdolność generowania prądu elektrycznego w ogniwie elektrochemicznym. Ostatecznie system nie został jednak wykorzystany w misjach kosmicznych, ze względu na niską gęstość uzyskiwanej mocy w stosunku do masy systemu oraz problemy ze stabilnością układu [6]. Do przełomowych wniosków w swoich badaniach doszedł Williams, który wykazał, że źródłem energii elektrycznej mogą być fermentujące odpady roślinne [29]. W swoim układzie w roli substratu wykorzystał łuski ryżu, które zostały poddane fermentacji beztlenowej. W swoim doświadczeniu Williams wygenerował 40 mA prądu o napięciu 6 V. Mimo stosunkowo wysokich prądów, rozwiązanie ograniczała niestabilność oraz niska sprawność układu.
Na początku lat 80. pojawiła się koncepcja wykorzystania MFC z mediatorami, czyli ze związkami redoks przenoszącymi elektrony z wnętrza komórek mikroorganizmów na powierzchnię anody (zastępują one bezpośredni transfer elektronów w przypadku bakterii pozbawionych efektywnego EET). Dodatkowo wykazano, że mediatory redukują się szybciej niż komórka produkuje elektrony, co oznacza, iż głównymi ograniczeniami MFC z mediatorem nie jest biologia komórki, a właściwości mediatora i elektrod [27].
Niezależnie od badań nad mediatorami, prowadzone były analizy zastosowania MFC z innymi substratami. W 1984 r., w wyniku zasilenia MFC odpadami zawierającymi laktozę, wykazano, że układ może pracować w systemie ciągłym przez dwa tygodnie, przy uzupełnianiu substratu [27]. W kolejnych latach udowodniono możliwość przetwarzania sacharozy w układzie z Proteus vulgaris oraz mediatorem w postaci tioniny, a także przetestowano w roli substratu ścieki i odpady węglowodanowe [3]. Pierwszą praktyczną demonstrację wykorzystania MFC w rzeczywistej oczyszczalni ścieków przeprowadzili Habermann i Pommer. W zaprojektowanym przez nich systemie MFC wykorzystano mikroorganizmy SRB (Sulfate-Reducing Bacteria), które generowały naturalny mediator, siarkowodór. Pozwoliło to na rezygnację z mediatorów syntetycznych, co ograniczyło koszty, a także zapewniło samowystarczalność układu. Układ Habermanna i Pommera działał w systemie pracy ciągłej przez pięć lat, co udowodniło, że MFC może być wykorzystane jako długoterminowa technologia do oczyszczania ścieków komunalnych [13].
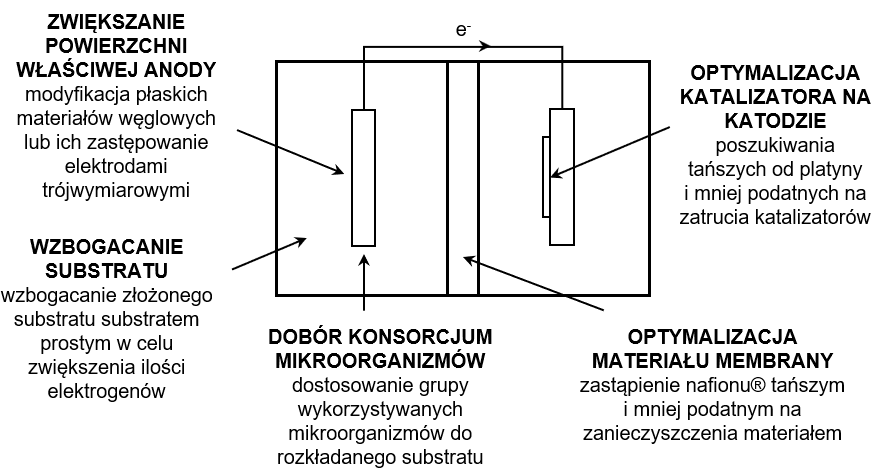
Fig. 2. Directions of MFC improvement, own study
Pod koniec lat 90. XX wieku wykazano, że bakterie redukujące metale tj. Shewanella putrefaciens, potrafią zasilić MFC bez egzogennych mediatorów. Kim w trakcie swoich badań wykazał elektroaktywność komórek Shewanella putrefaciens hodowanych beztlenowo oraz generację prądu z mleczanu przy braku barwników redoks, co interpretowano jako bezpośredni kontaktowy transfer elektronów (DET) przez zewnętrzne cytochromy do anody Choć Shewanella putrefaciens utleniały mleczan niecałkowicie, co prowadziło do wytwarzania nieznacznej ilości energii, wskazało to zdolność niektórych mikroorganizmów do bezpośredniego przenoszenia elektronów do elektrod [18].
3. Optymalizacja i doskonalenie układów MFC
Efektywność MFC zależy od parametrów i dopasowania poszczególnych komponentów systemu, tj. elektrod, membran, wykorzystanych mikroorganizmów i substratów. Na przestrzeni lat optymalizowano poszczególne elementy układu i tworzono różne konfiguracje po to, by uzyskać jak najlepsze parametry pracy systemu (rys. 2). Choć w początkowych MFC używano mikroorganizmy bez rozwiniętego DET, na przełomie XX i XXI wieku zaczęto poszukiwać bakterii cechujących się bezpośrednim kontaktowym transferem elektronów, co umożliwiało całkowitą rezygnację z wykorzystania mediatorów syntetycznych. Przy wykorzystaniu Geobacter sulfurreducens w MFC wykazano, że mikroorganizm tworzy stabilny biofilm na anodzie i podtrzymuje prąd po pełnej wymianie pożywki [4]. Wśród najbardziej znanych egzoelektrogenów wyróżnia się również mikroorganizmy z rodziny Shewanella [18].
W przypadku wykorzystania substratu złożonego, materia organiczna musi w pierwszej kolejności zostać zhydrolizowana do cukrów prostych, następnie sfermentowana do lotnych kwasów tłuszczowych, a w ostatnim etapie – utleniona przez egzoelektrogeny. Dla celulozy komponentem hydrolityczno-fermentacyjnym jest np. Clostridium cellulolyticum. Przy wytwarzaniu energii elektrycznej w MFC z wykorzystaniem otrębów ryżowych (60% poliacharydów), możliwe jest zastosowanie konsorcjum mikroorganizmów, w którym Clostridium degraduje polimerową celulozę do glukozy, część glukozy jest fermentowana do kwasów organicznych przez Clostridium i Bacteroides, a następnie kwasy te są zużywane przez Geobacter do transferu elektronów na anodę [32]. Substrat w postaci pulpy ziemniaczanej może być rozkładany przez hydrolityczno-fermentacyjne bakterie z rodzajów Bacteroides, Flavobacterium (rozkład skrobi) oraz Ruminococcus (rozkład celulozy) [28].
Proces adaptacji mikroorganizmów zwiększa efektywność wytwarzania energii przez MFC wykorzystujące ścieki bytowe. Wzbogacanie w Geobacter sulfurreducens, poprzez dodanie do ścieków octanu, zwiększa wydajność kulombowską, ale nie całkowitą produkcję prądu, która nie może się odbywać w wyniku braku wystarczającej ilości hydrolizatorów i fermentatorów [11].
Jedną z metod poprawy wydajności MFC jest zwiększenie powierzchni właściwej anody, co umożliwia efektywniejszą kolonizację bakterii egzoelektrogenicznych i, tym samym, zwiększa transfer elektronów. Konieczne jest przy tym uwzględnienie porowatości materiału, ponieważ zbyt małe pory tj. 2–7 μm, jak np. w piance węglowej, są zatykane przez biofilm, co prowadzi do obumierania bakterii wewnątrz oraz spadku generowanej mocy. Wykorzystanie anody szczotkowej, składającej się z wielu cienkich włókien węglowych, pozwoliło na zwiększenie maksymalnej gęstości mocy z 1070 mW/m2, osiąganej przez MFC z anodą z tkaniny węglowej, do 2400 mW/m2, co wynikało m.in. ze wzrostu efektywnej powierzchni anody oraz redukcji oporu wewnętrznego MFC [23].
Dla zwiększenia efektywności materiałów węglowych zaproponowano także nanorurki węglowe (CNT), które pozwoliły na osiągnięcie o 68% wyższej maksymalnej gęstości mocy od analogicznego MFC wykorzystującego anodę z tkaniny węglowej. Nanorurki węglowe są jednak toksyczne dla mikroorganizmów, ponieważ uszkadzają struktury błon komórkowych, [17].
Testując możliwości poprawy wydajności MFC wykazano, że poddanie anody węglowej obróbce amoniakiem w wysokiej temperaturze skutkuje wprowadzeniem grup zawierających azot na powierzchnię, co zwiększa reaktywność powierzchni [23].
Dla poprawy efektywności MFC korzystna jest modyfikacja grafenem, co wynika m.in. z wysokiej przewodności i dużej powierzchni właściwej materiału. Dla grafenu pozyskiwanego w redukcji chemicznej powierzchnia właściwa jest większa od powierzchni filcu grafitowego ok. 500 razy [33].
Zwiększanie chropowatości powierzchni i poprawa przewodności powierzchni elektrody możliwe jest również poprzez modyfikację anody polimerami. Modyfikacja anody z filcu węglowego materiałami polimerowymi pozwoliła na zwiększenie gęstości mocy względem MFC z anodą niemodyfikowaną o 35% dla polianiliny PANI oraz o 18% dla polimeru PAOA. Wynika to m.in. z szybszego zasiedlenia anod przez bakterie, poprawy różnorodności mikrobiologicznej na anodach modyfikowanych oraz redukcji oporu wewnętrznego [20].
Biomasa roślinna po odpowiedniej obróbce termicznej zostaje przekształcona w węgiel porowaty, który może znaleźć zastosowanie jako efektywny i niskokosztowy materiał elektrodowy. Porównanie anody z biocharu aktywowanego KOH i nieaktywowanego wykazało, że aktywacja materiału, w wyniku wytworzenia mezoporowej struktury na powierzchni elektrody, zwiększa dwukrotnie osiągane przez MFC gęstości mocy, które mogą przewyższać gęstości mocy osiągane przez materiały konwencjonalne tj. filc grafitowy [31]. Wykorzystanie anody z łupin kasztanów poddanych karbonizacji i aktywacji w MFC pozwoliło na uzyskanie 2,3-razy większej gęstości mocy od analogicznego układu wykorzystującego tkaninę węglową [10]. Anoda z węgla pochodzącego z odpadów kawowych w układzie MFC doprowadziła do osiągnięcia maksymalnej gęstości mocy równej 3800 mW/m2 [14].
Kluczowym elementem warunkującym efektywność MFC jest katoda. Jako, że, zachodząca na niej, reakcja redukcji tlenu ORR jest powolna i stanowi czynnik limitujący osiąganą moc, współcześnie wykorzystuje się katalizatory przyśpieszające przebieg procesu. Standardowe katalizatory platynowe, choć cechują się wysoką aktywnością w ORR, są drogie i podatne na zatrucia siarkowodorem, co prowadzić może do zaniku stabilności MFC [5]. Wykazano, że dobrymi właściwościami katalitycznymi charakteryzuje się tlenek manganu o strukturze krystalicznej OMS-2 (Octahedral Molecular Sieve-2). Domieszkowanie kobaltem lub miedzią pozwoliło na zwiększenie efektywności katalizatora MnO2 i uzyskanie gęstości mocy wyższych niż w przypadku zastosowania tradycyjnych katalizatorów platynowych. Katalizator MnO2 z domieszkami wykazuje się również dwukrotnie wyższym parametrem usuwania COD, jest znacznie tańszy od platyny i bardziej odporny na zatrucia [24].
Dla redukcji kosztów katalizatorów oraz zwiększenia efektywności ORR na katodzie wykorzystać można również stopy platyny z innymi metalami. Katalizator Pt-Ni w MFC umożliwił wytworzenie gęstości mocy 3,5-krotnie wyższej niż miało to miejsce przy wykorzystaniu katalizatora platynowego, co było wynikiem synergicznego działania platyny i niklu w stopie prowadzącego do obniżenia nadpotencjału redukcji tlenu [7].
Od początku rozwoju technologii MFC, najpopularniejszym materiałem wykorzystywanym w roli membrany PEM jest Nafion®, czyli perfluorowany polimer kwasu sulfonowego, co wynika z wysokiej przewodności protonowej oraz stabilności chemicznej i termicznej materiału. W związku z wykazaniem niekorzystnych cech Nafionu tj. wyciek tlenu na anodę, preferencyjny transport występujących w dużych stężeniach kationów i ich reakcja na katodzie, strata substratu i zanieczyszczenie biofilmem po dłuższym czasie eksploatacji oraz wysokimi kosztami tego materiału zaczęto testować możliwość wykorzystania w roli membrany innych materiałów [8].
Jedną z pierwszych alternatyw były membrany sulfonowe powstałe na bazie polimerów aromatycznych. Sulfonowany polieteroeteroketon SPEEK jest polimerem, który po wprowadzeniu grup sulfonowych –SO3H, zyskuje zdolność przewodzenia protonów. Dla uzyskania odpowiednio wysokiego przewodnictwa konieczne jest zapewnienie wysokiego stopnia sulfonowania DS, który jednak może powodować pęcznienie i rozpuszczanie polimeru, co obniża jego wytrzymałość i stabilność chemiczną [21].
Dużą grupę stanowią membrany porowate, które, choć fizycznie oddzielają komory anodową i katodową, nie posiadają aktywnych grup jonowymiennych, w związku z czym transport ładunku odbywa się poprzez swobodną dyfuzję wszystkich jonów przez wypełnione elektrolitem pory. Cechują się nieselektywnością jonową, w wyniku czego przenoszone mogą być zarówno kationy, jak i aniony, zgodnie z gradientem stężeń [26]. Przykład membran porowych stanowią niskokosztowe membrany tekstylne, tj. J-cloth. Materiał wykazuje się dobrą przepuszczalnością dla jonów oraz łatwą dostępnością, jednak jego sprawność kulombowska jest niska w porównaniu do innych separatorów [34].
Do membran porowatych zalicza się również membrany ceramiczne. W wyniku spiekania gliny naturalnej tworzy się porowata struktura umożliwiająca transport protonów poprzez ich przeskakiwanie między ujemnie naładowanymi grupami tj. krzemiany i gliniany. Jedną z głównych wad membran ceramicznych jest występowanie zjawiska odkładania się biofilmu na katodzie, co wynika m.in. z wysokiej porowatości materiału i braku selektywności jonowej w membranie [15].
Dla obniżenia kosztów i uproszczenia konstrukcji MFC możliwe jest wykorzystanie układu pozbawionego membrany. Do zalet tego typu rozwiązania zalicza się redukcję całkowitej rezystancji układu, co wynika z wyeliminowania oporu membrany i zapewnienia swobodnego przemieszczania się protonów i innych kationów w całej objętości ogniwa. Opracowane ogniwo jednokomorowe z katodą powietrzną, pozbawione membrany polimerowej i substratem w postaci glukozy umożliwiło uzyskanie gęstość mocy 494 mW/m², co stanowiło wartość niemal dwukrotnie większą od otrzymywanych gęstości mocy w tradycyjnych, dwukomorowych układach z membraną PEM [22]. Ze względu na dyfuzję tlenu na anodzie szacuje się, że MFC pozbawione membrany osiągają sprawność kulombowską niższą od układów konwencjonalnych o ok. 20% [19].
4. Wyzwania stojące przed wdrożeniem MFC
Jednym z obszarów zastosowań MFC są biosensory, które wykorzystują zależność pomiędzy generowanym sygnałem elektrycznym a biochemicznym zapotrzebowaniem na tlen BOD, chemicznym zapotrzebowaniem na tlen COD lub stężeniem substancji toksycznych. Konstruowane są również czujniki zanurzalne, które cechują się możliwością mierzenia BOD zbiorników wodnych, co eliminuje konieczność pobierania próbek i przeprowadzania konwencjonalnych testów laboratoryjnych. Czujniki oparte na MFC wykazują jednak ograniczone m.in. przez zmieniającą się w czasie strukturę biofilmu na elektrodach oraz obecność substancji toksycznych zaburzających sygnał elektryczny [30].
Innym kierunkiem rozwoju współczesnych MFC jest wykorzystanie ich jako źródeł energii dla rozproszonych urządzeń. Dzięki zdolności do wykorzystywania materii organicznej pochodzącej m.in. z osadów dennnych, gleb lub ścieków, MFC może zapewnić długotrwałe zasilanie off-grid. Glebowe MFC z anodą pod powierzchnią ziemi oraz katodą ulokowaną na jej powierzchni mogą być wykorzystywane do zasilania sieci czujników bezprzewodowych. Ciągłe zasilanie urządzeń wyłącznie z MFC jest możliwe jednak tylko dla sprzętu o bardzo niskim zapotrzebowaniu energetycznym [16].
Ze względu na możliwość jednoczesnego usuwania zanieczyszczeń organicznych i odzysk energii, jednym z najbardziej obiecujących obszarów rozwoju MFC są oczyszczalnie ścieków. W ostatnich latach przeprowadzono szereg pilotażowych wdrożeń, które miały na celu ocenić wydajność tej technologii w warunkach zbliżonych do rzeczywistych. Jednym z nich jest technologia BETT (z ang. Bioelectrochemical Treatment Technology). BETT opiera się na modułowym systemie MFC w układzie przepływowym, których głównym zadaniem jest oczyszczanie ścieków przemysłowych oraz redukcja emisji CO2. Składa się on z 28 połączonych szeregowo jednostek anodowych, które wykonane zostały z przewodzącego rdzenia pokrytego materiałem z włókna węglowego. Do układu szeregowo podłączone są dwie powietrzne katody. Układ pilotażowy, złożony z 12 układów BETT, zbiorników wyrównawczych, zasilających i zbiorczych, przetestowano w USA na przepływie ścieków browarniczych wynoszącym 0,6 m3/d. Przy hydraulicznym czasie retencji HRT równym 4h osiągnięto efektywność usuwania COD wynoszącą 33% oraz całkowitej zawiesiny TSS 79%. Zmierzona gęstość mocy układu BETT wyniosła 114 mW/m2 [2]. W podobny sposób układ MFC wykorzystano do oczyszczania odpadów trzody chlewnej w Kalifornii. Układ złożony z 12 jednokomorowych MFC połączonych szeregowo wykazał efektywność usuwania COD do 65% oraz odzysk energii netto wynoszący 0,11 kWh/kg COD [1].
Mimo korzyści MFC, masowe wdrożenie tej technologii w oczyszczalniach i zakładach przemysłowych wymaga przezwyciężenia licznych wyzwań. Jedną z podstawowych trudności jest skalowanie, które prowadzi do wzrostu oporów wewnętrznych wynikających m.in. z dłuższej drogi jonów w większych komorach i gorszej dyfuzja substratu do głębszych warstw biofilmu, a także do problemów z jednorodnością warunków w reaktorze. Pilotażowe MFC wykazują dużą zmienność wydajności w zależności od warunków środowiskowych tj. zmiany pH, temperatura i obciążenie organiczne [9]. MFC jednak wciąż stanowią technologię rozwijającą się, a postęp w obszarze materiałoznawstwa i technologii może stopniowo eliminować bariery, czyniąc MFC konkurencyjnym i zrównoważonym rozwiązaniem w gospodarce odpadami i w zasilaniu urządzeń.
Literatura
[1] Chakma, R., Hossain, M. K., Paramasivam, P., Bousbih, R., Amami, M., Toki, G. I., Haldar, R., & Karmaker, A. K. (2025). Recent applications, challenges, and future prospects of microbial fuel cells: A review. Global Challenges, 9(5). https://doi.org/10.1002/gch2.202500004
[2] Potter, M. C. (1911). Electrical effects accompanying the decomposition of organic compounds. Proceedings of the Royal Society B: Biological Sciences, 84(571), 260–276.
[3] Cohen, B. (1931). The bacterial culture as an electrical half-cell. Journal of Bacteriology, 21, 18–19.
[4] Canfield, J. H., Goldner, B. H., & Lutwack, R. (1963). Research on applied bioelectrochemistry. Report no. 1. Utilization of human wastes as electrochemical fuels. Magna Corporation; National Aeronautics and Space Administration.
[5] Williams, K. R. (1966). An introduction to fuel cells. Elsevier Publishing Company.
[6] Roller, S. D., Bennetto, H. P., Delaney, G. M., Mason, J. R., Stirling, J. L., & Thurston, C. D. (1984). Electron-transfer coupling in microbial fuel cells, 1: Comparison of redox mediator reduction rates and respiratory rates of bacteria. Journal of Chemical Technology and Biotechnology, 34(1), 3–12.
[7] Bennetto, H. P., Delaney, G. M., Mason, J. R., Roller, S. D., Stirling, J. L., Thurston, C. F., & White, D. R., Jr. (1986). An electrochemical bioreactor for treatment of carbohydrate wastes and effluents. Alternative Energy Sources, 4, 143–157.
[8] Habermann, W., & Pommer, E. H. (1991). Biological fuel cells with sulphide storage capacity. Applied Microbiology and Biotechnology, 35(1), 128–133.
[9] Kim, B. H., Kim, H. J., Hyun, M. S., & Park, D. H. (1999). Direct electrode reaction of Fe(III)-reducing bacterium, Shewanella putrefaciens. Journal of Microbiology and Biotechnology, 9(2), 127–131.
[10] Bond, D. R., & Lovley, D. R. (2002). Electricity production by Geobacter sulfurreducens attached to electrodes. Applied and Environmental Microbiology, 69(3), 1548–1555.
[11] Yoshimura, Y., Nakashima, K., Kato, M., Inoue, K., Okazaki, F., Soyama, H., & Kawasaki, S. (2018). Electricity generation from rice bran by a microbial fuel cell and the influence of hydrodynamic cavitation pretreatment. ACS Omega, 3(11), 15267–15271. https://doi.org/10.1021/acsomega.8b02171
[12] Tian, Y., Mei, X., Liang, Q., Wu, D., Ren, N., & Xing, D. (2017). Biological degradation of potato pulp waste and microbial community structure in microbial fuel cells. RSC Advances, 7, 8376–8380. https://doi.org/10.1039/C6RA28599A
[13] Christgen, B., Spurr, M., Milner, E. M., Izadi, P., McCann, C., Yu, E., Curtis, T., Scott, K., & Head, I. M. (2023). Does pre-enrichment of anodes with acetate to select for Geobacter spp. enhance performance of microbial fuel cells when switched to more complex substrates? Frontiers in Microbiology, 14, 1199286. https://doi.org/10.3389/fmicb.2023.1199286
[14] Logan, B. E., Cheng, S., Watson, V., & Estadt, G. (2007). Graphite fiber brush anodes for increased power production in air-cathode microbial fuel cells. Environmental Science & Technology, 41(9), 3341–3346.
[15] Karwowska, E., Miaśkiewicz-Pęcka, E., & Załęska-Radziwiłł, M. (2015). Wpływ nanoproduktów na wybrane organizmy – ocena ekotoksykologiczna. Inżynieria i Ochrona Środowiska, 18(1), 109–118.
[16] Li, C., Zhang, L., Ding, L., Ren, H., & Cui, H. (2011). Effect of conductive polymers coated anode on the performance of a microbial fuel cell (MFCs) and its biodiversity analysis. Biosensors and Bioelectronics, 26(10), 4169–4176.
[17] Yin, H., Zhang, M., Xu, X., & Chen, X. (2025). Modulation of biomass-based anode specific surface area and electrical conductivity on the enhancement of microbial fuel cell power generation capacity. Journal of Chemical Technology & Biotechnology. https://doi.org/10.1002/jctb.70097
[18] Chen, Q., Pu, W., Hou, H., Hu, J., Liu, B., Li, J., Cheng, K., Huang, L., Yuan, X., Yang, C., & Yang, J. (2018). Activated microporous–mesoporous carbon derived from chestnut shell as a sustainable anode material for high performance microbial fuel cells. Bioresource Technology, 249, 567–573.
[19] Hung, Y.-H., Liu, T.-Y., & Chen, H.-Y. (2019). Renewable coffee waste-derived porous carbons as anode materials for high-performance sustainable microbial fuel cells. ACS Sustainable Chemistry & Engineering, 7(20), 16991–16999.
[20] Brouzgou, A., Song, S. Q., & Tsiakaras, P. (2012). Low and non-platinum electrocatalysts for PEMFCs: Current status, challenges and prospects. Applied Catalysis B: Environmental, 127, 371–388.
[21] Lu, M., Kharkwal, S., Ng, H. Y., & Li, S. F. Y. (2010). Carbon nanotube supported MnO₂ catalysts for oxygen reduction reaction and their applications in microbial fuel cells. Biosensors and Bioelectronics, 26(12), 4728–4732.
[22] Cetinkaya, A. Y., Ozdemir, O. K., Koroglu, E. O., Hasimoglu, A., & Ozkaya, B. (2015). The development of catalytic performance by coating Pt–Ni on CMI7000 membrane as a cathode of a microbial fuel cell. Bioresource Technology, 195, 188–193.
[23] Chae, K.-J., Choi, M.-J., Lee, J., Kim, I. S., & Kim, K. Y. (2007). Effect of proton exchange membranes on performance of microbial fuel cells. Journal of Power Sources, 171(2), 348–354.
[24] Li, L., Zhang, J., & Wang, Y. (2003). Sulfonated poly(ether ether ketone) membranes for direct methanol fuel cells. Journal of Membrane Science, 226(1–2), 159–167.
[25] Ramírez-Nava, J., Martínez-Castrejón, M., García-Mesino, R. L., López-Díaz, J. A., Talavera-Mendoza, O., Sarmiento-Villagrana, A., Rojano, F., & Hernández-Flores, G. (2021). The implications of membranes used as separators in microbial fuel cells. Membranes, 11(10), 738. https://doi.org/10.3390/membranes11100738
[26] Zhang, X., Cheng, S., Wang, X., Huang, X., & Logan, B. E. (2009). Separator characteristics for increasing performance of microbial fuel cells. Environmental Science & Technology, 43(21), 8456–8461.
[27] Liu, H., & Logan, B. E. (2004). Electricity generation using an air-cathode single chamber microbial fuel cell in the presence and absence of a proton exchange membrane. Environmental Science & Technology, 38(14), 4040–4046.
[28] Leong, J. X., Wan Daud, W. R., Ghasemi, M., Liew, K. B., & Ismail, M. (2013). Ion exchange membranes as separators in microbial fuel cells for bioenergy conversion: A comprehensive review. Renewable and Sustainable Energy Reviews, 28, 575–587.
[29] Yao, H., Xiao, J., & Tang, X. (2023). Microbial fuel cell-based organic matter sensors: Principles, structures and applications. Bioengineering, 10(8), 886. https://doi.org/10.3390/bioengineering10080886
[30] Jalili, P., Ala, A., Nazari, P., Jalili, B., & Domiri Ganji, D. (2024). A comprehensive review of microbial fuel cells considering materials, methods, structures, and microorganisms. Heliyon, 10(3), e25439. https://doi.org/10.1016/j.heliyon.2024.e25439
[31] Babanova, S., Jones, J., Wiseman, K., Soles, J., Gracia, J., Huerta, P., Barocio, D., Naito, R., Arreola, O., Gracia, G., & Bretschger, O. (2022). Bioelectrochemical treatment technology—The new practical approach for wastewater management and GHG emissions reduction. Frontiers in Chemical Engineering, 4, 832505. https://doi.org/10.3389/fceng.2022.832505
[32] Babanova, S., Jones, J., Phadke, S., Lu, M., Angulo, C., Gracia, J., Carpenter, K., Cortese, R., Chen, S., Phan, T., & Bretschger, O. (2020). Continuous flow, large-scale, microbial fuel cell system for the sustained treatment of swine waste. Water Environment Research, 92(1), 60–67. https://doi.org/10.1002/wer.1183
[33] Jadhav, D. A., Park, S.-G., Eisa, T., Mungray, A. K., Madenli, E. C., Olabi, A.-G., Abdelkareem, M. A., & Chae, K.-J. (2022). Current outlook towards feasibility and sustainability of ceramic membranes for practical scalable applications of microbial fuel cells. Renewable and Sustainable Energy Reviews, 167, 112708
