Afiliacja
1 Politechnika Krakowska im. Tadeusza Kościuszki, Wydział Inżynierii Środowiska i Energetyki, Katedra Technologii Środowiskowych,
*Kontakt / Correspondence: klaudia.kwiatkowska@pk.edu.pl
DOI: 10.65545/GWITS.2026.01.02, GWiTS 1/2026, styczeń 2025
Pobierz PDF (Open Access)
Streszczenie:
Jednym z najistotniejszych problemów związanych z eksploatowaniem instalacji wodnych jest powstawanie i osadzanie się biofilmów mikrobiologicznych. Obecność tych struktur wpływa bezpośrednio na jakość wody, rozwój organizmów patogennych oraz zapoczątkowanie procesu korozji systemów. W konsekwencji dochodzi do zmniejszenia efektywności systemów hydraulicznych doprowadzających wodę do odbiorców. Biofilmy w instalacjach wodnych są złożonymi, wielogatunkowymi konsorcjami mikroorganizmów, w których kluczową rolę odgrywają interakcje komórkowe oraz procesy molekularne regulujące adhezję, produkcję macierzy pozakomórkowej (EPS) i organizację struktury przestrzennej. W pracy omówiono aktualny stan wiedzy dotyczący mechanizmów tworzenia biofilmów, czynników środowiskowych wpływających na ich stabilność oraz zakres metod kontroli i usuwanie biofilmów. Szczególną uwagę zwrócono na metody fizyczne, chemiczne, enzymatyczne, a także modyfikacje powierzchni materiałów instalacyjnych.
Słowa kluczowe: biofilm, zanieczyszczenie mikrobiologiczne, instalacje wodne, jakość wody
Abstract:
One of the most significant problems associated with the operation of water systems is the formation and deposition of microbial biofilms. The presence of these structures directly affects water quality, the growth of pathogenic organisms, and the initiation of corrosion processes in the systems. As a result, the efficiency of hydraulic systems supplying water to consumers is reduced. Biofilms in water systems are complex, multi-species consortia of microorganisms in which cellular interactions and molecular processes regulating adhesion, extracellular matrix (EPS) production, and spatial structure organization play a key role. The paper discusses the current state of knowledge on the mechanisms of biofilm formation, environmental factors affecting their stability, and the range of methods for controlling and removing biofilms. Particular attention is paid to physical, chemical, and enzymatic methods, as well as modifications to the surface of installation materials.
Keywords: biofilm, microbial contamination, water installations, water quality
1. Wstęp
Biofilmy, które mogą występować w instalacjach wodnych, stanowią jeden z kluczowych problemów łączących mikrobiologię środowiskową, inżynierię sanitarną oraz bezpieczeństwo zdrowia publicznego. Biofilm definiowany jest jako złożona, trójwymiarowa populacja komórek, które są owinięte matrycą EPS (Extracellular Polymeric Substances) [1]. Mają również zdolność do adhezji do powierzchni stałej, która następuje w kontakcie z wodą. Z tego względu, w warunkach instalacji wodociągowych, biofilm jest zjawiskiem bardzo często spotykanym, który wynika z zachodzenia naturalnych procesów mikrobiologicznych. W obecności wody, substancji odżywczych i dostępu do powierzchni instalacji wodnych dochodzi do kolonizacji i rozwoju biofilmu, a więc wielogatunkowych struktur biologicznych, w których zachodzą procesy fizjologiczne i molekularne [2].
Biofilm nie jest jedynie zlepkiem komórek bakteryjnych. Jest to zorganizowany, dynamicznie rozwijający się ekosystem, którego właściwości i zachowanie różnią się znacząco w zależności od składu gatunkowego. W obrębie biofilmu mikroorganizmy znajdują się w stanie wysokiego zróżnicowania metabolicznego, wykorzystując złożoną sieć interakcji międzygatunkowych opartych na konkurencji, kooperacji i komunikacji chemicznej [1].
Szczególnie w instalacjach wodnych znaczenie biofilmów w kontekście mikrobiologicznym jest kluczowe. Jest to związane z możliwością stania się rezerwuarem dla drobnoustrojów patogennych oraz oportunistycznych, takich jak Legionella pneumophila, Pseudomonas aeruginosa , czy wolno rosnące mykobakterie [3]. Ponadto biofilmy mogą uczestniczyć w procesach korozji, zaburzać jakość fizykochemiczną wody oraz wpływać na efektywność zastosowanych procesów dezynfekcji wody. Z tego względu zrozumienie mechanizmów formowania biofilmów jest kluczowe dla opracowania skutecznych strategii prewencji i kontroli [4].
Celem niniejszego artykułu jest przedstawienie mikrobiologicznych podstaw powstawania biofilmów w instalacjach wodnych, ze szczególnym uwzględnieniem etapów adhezji komórek, regulacji molekularnej oraz procesów prowadzących do dojrzewania i dyspersji biofilmu. Poznanie mechanizmów funkcjonowania biofilmów stanowi fundament dla zrozumienia, dlaczego te struktury są tak trudne do eliminacji oraz jakie warunki sprzyjają ich utrwalaniu się w środowisku wodnym.
2. Mechanizm powstawania biofilmów
Mechanizm formowania biofilmów jest procesem wieloetapowym, w którym uczestniczą czynniki mikrobiologiczne, fizykochemiczne oraz właściwości materiałów konstrukcyjnych instalacji. W początkowej fazie tworzenia biofilmu, mikroorganizmy są luźno i odwracalnie przyczepione do powierzchni, w sposób polarny [5]. Już w pierwszych sekundach kontaktu dochodzi do szeregu oddziaływań molekularnych, warunkujących dalsze etapy kolonizacji. W środowisku wodnym odpowiedzialne za inicjację adhezji są głównie siły Van der Waalsa, związki hydrofobowe oraz ładunki elektrostatyczne, które determinują stopień przyciągania komórek do powierzchni instalacji. Materiały wykorzystywane w systemach hydraulicznych różnią się chropowatością, energią powierzchniową i skłonnością do gromadzenia osadów, co znacząco wpływa na intensywność kolonizacji [6].
Wkrótce po pomyślnej adhezji mikroorganizmów do powierzchni, przylegające mikroorganizmy rozpoczynają namnażanie i agregację w obrębie samodzielnie wyprodukowanego EPS, prowadząc do powstania mikrokolonii [7]. W tym etapie EPS odgrywa kluczową rolę, ponieważ umożliwia dojrzewanie biofilmu, poprzez stabilizowanie trójwymiarowej struktury biofilmu, grupowanie komórek oraz ochronę przed różnymi stresorami. Dojrzały biofilm może uzyskać strukturę w kształcie „grzyba” lub „wieży”, w której mikroorganizmy są ułożone zgodnie z tempem metabolizmu. Tak powstały dojrzały biofilm ma strukturę trójwarstwową: wewnętrzną warstwę regulującą, środkową warstwę składającą się z drobnoustrojów oraz warstwę zewnętrzną tworzoną przez mikroorganizmy gotowe do opuszczenia biofilmu [8] (rys. 1). Stworzony układ pełni funkcję stabilizującą i ochronną, ponieważ zapewnia komórkom retencję wody i substancji odżywczych, a także chroni przed stresem termicznym i chemicznym. W biofilmie zachodzi jednocześnie reorganizacja przestrzenna, ponieważ komórki łączą się w mikrokolonie, między którymi tworzą się kanały umożliwiające cyrkulację wody i dyfuzję metabolitów. Instalacje wodne, dzięki zmiennemu przepływowi, różnicom temperatury i możliwości gromadzenia się cząstek organicznych, sprzyjają powstawaniu heterogenicznych struktur o zróżnicowanych warunkach tlenowych i redoks [7].
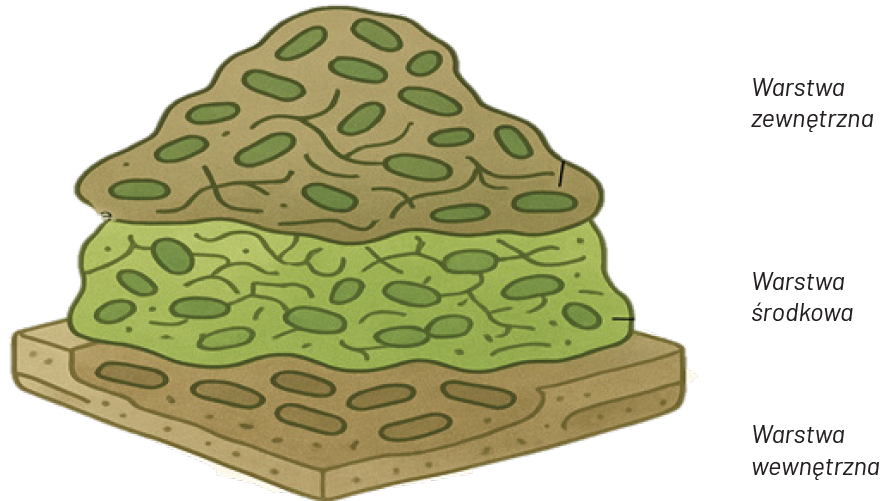
Fig. 1. Diagram of a mature biofilm, own elaboration
W momencie kontaktu z powierzchnią, mikroorganizmy uruchamiają mechanizmy ułatwiające stabilizację adhezji. Istotną rolę odgrywają fimbrie typu IV, białka adhezyjne oraz substancje o charakterze mukopolisacharydowym, które ulegają ekspresji w odpowiedzi na sygnały środowiskowe [9]. Po fazie adhezji odwracalnej następuje etap trwałego przytwierdzenia, związany z przeorganizowaniem ekspresji genów. Jednym z kluczowych regulatorów w tym procesie jest cykliczny di-GMP (c-di-GMP), którego wysokie stężenie sprzyja zahamowaniu ruchliwości komórki i zwiększeniu syntezy komponentów macierzy pozakomórkowej. Wzrost poziomu c-di-GMP stanowi sygnał do formowania wielowarstwowej, stabilnej struktury. Rozwój biofilmu wiąże się także z zaawansowaną komunikacją międzykomórkową [10]. Mikroorganizmy w biofilmie wykorzystują mechanizmy quorum sensing (QS), oparte na cząsteczkach sygnałowych takich jak acylowane homoserynolaktany (AHL), autoinduktory peptydowe (AIP) oraz autoinduktor-2 (AI-2). Sygnały te regulują ekspresję genów odpowiedzialnych za produkcję EPS, syntezę biofilmotwórczych enzymów, tolerancję na stres oksydacyjny oraz odporność na środki dezynfekcyjne. Dzięki QS biofilm staje się strukturą zorganizowaną, w której różne populacje mikroorganizmów mogą synchronizować swoje zachowania i dostosowywać je do warunków panujących w instalacji [11]. Komunikacja ta sprzyja jednocześnie utrzymywaniu zrównoważonego układu ekologicznego, w którym współistnieją bakterie tlenowe, mikroaerofilne i beztlenowe. W dojrzewającym biofilmie ważną rolę odgrywają gradienty środowiskowe. Na powierzchni biofilmu dominują bakterie intensywnie metabolizujące i dobrze dotlenione, podczas gdy wewnętrzne warstwy zamieszkują mikroorganizmy o obniżonym metabolizmie. Takie komórki wykazują wyjątkową tolerancję na biocydy oraz wysoką zdolność przetrwania niekorzystnych warunków. Zróżnicowanie to sprzyja również powstawaniu nisz ekologicznych dla patogenów, takich jak Legionella pneumophila, która preferuje warunki mikroaerofilne [12].
Ostatnim etapem cyklu życia biofilmu jest jego dyspersja [9]. Proces ten może być wywołany zmianami środowiska, działaniem biocydów, stresem mechanicznym lub aktywacją bakteryjnych enzymów degradujących EPS, takich jak nukleazy czy proteazy. Dyspersja prowadzi do uwalniania komórek w formie pojedynczej lub agregatowej, które mogą kolonizować nowe odcinki instalacji, a także przedostawać się do użytkowej wody. Uwolnione komórki często cechują się zwiększoną wirulencją i zdolnością szybkiego przylegania, co stanowi realne zagrożenie epidemiologiczne [13]. W ostatnim etapie rozwoju biofilm osiąga tzw. krytyczną grubość i stopniowo przestaje utrzymywać istniejącą formę. Następuje wówczas migracja komórek z peryferyjnych części dojrzałego biofilmu do otoczenia [9] (rys. 2). Prawdopodobnie dochodzi do degradacji polimerowej matrycy, aktywacji aparatów ruchowych i zmian fizjologicznych w komórkach, umożliwiających ich egzystencję poza biofilmem. Przypuszcza się także, że odłączanie komórek od biofilmu i jego dyspersja jest celową separacją, wynikającą z reakcji na niesprzyjające zmiany środowiskowe. Przyczyną tego zjawiska może być wyczerpanie składników pokarmowych lub problemy ich przepływu w obrębie biofilmu. W ten sposób biofilm przystosowuje się do zmian środowiskowych, a oderwane komórki rozpoczynają proces kolonizacji nowych powierzchni [14].
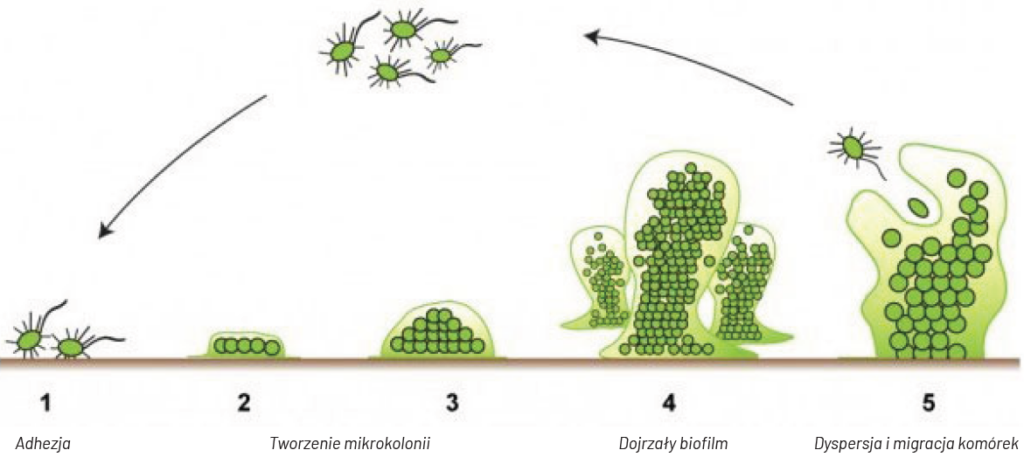
Fig. 2. Biofilm formation diagram [21]
3. Czynniki wpływające na tempo i stabilność formowania biofilmów
Złożoność czynników wpływających na tempo formowania biofilmów w instalacjach wodnych sprawia, że proces ten jest dynamiczny oraz bardzo często trudny do przewidzenia. W związku z tym wymaga przestrzegania reżimu eksploatacyjnego, wraz z odpowiednio wdrożonymi strategiami prewencyjnymi. Tylko całościowe podejście, uwzględniające właściwości wody, konstrukcję instalacji, parametry eksploatacyjne oraz biologię mikroorganizmów, pozwala skutecznie kontrolować rozwój biofilmów [15].
Za najważniejszy czynnik determinujący szybkość powstawania biofilmów uważany jest skład fizykochemiczny wody, w szczególności obecność substancji organicznych i mikroelementów. Nawet niewielkie stężenia węgla organicznego (TOC) potrafią stymulować wzrost bakterii heterotroficznych. Obecność związków azotu, fosforu i żelaza zapewnia źródło składników odżywczych, przyspieszając tworzenie mikrokolonii. Z kolei wysoka twardość wody sprzyja odkładaniu się węglanu wapnia, który zwiększa chropowatość powierzchni, przyspieszając tym samym adhezję bakterii [16].
Temperatura wody również odgrywa znaczącą rolę, ponieważ warunkuje aktywność enzymatyczną i tempo metabolizmu mikroorganizmów. To właśnie w instalacjach ciepłej wody użytkowej (30–50°C) wzrost biofilmów zachodzi najbardziej intensywnie, ponieważ zakres ten sprzyja rozwojowi wielu bakterii środowiskowych. Obniżenie temperatury spowalnia rozwój biofilmu, ale go całkowicie nie hamuje, ponieważ niektóre mikroorganizmy potrafią funkcjonować nawet przy 4–10°C, szczególnie te o strategii przetrwalnej [4].
Bardzo istotnym parametrem jest także prędkość i charakter ruchu wody. Zbyt niski przepływ sprzyja sedymentacji cząstek organicznych oraz umożliwia komórkom długotrwały kontakt z powierzchnią, co prowadzi do szybkiego przytwierdzania i rozpoczęcia procesu adhezji biofilmu [17]. Z drugiej strony, zastosowanie przepływu turbulentnego, utrudniającego działanie na wczesną adhezję, sprzyja dojrzewaniu biofilmu, poprzez dostarczanie tlenu i składników odżywczych do głębszych warstw [18]. Z tego względu te instalacje, które przez dłuższy czas pozostają nieużytkowane lub poddane stagnacji, stwarzają środowisko sprzyjające gwałtownemu narastaniu biofilmów. Również materiał konstrukcyjny instalacji to czynnik mający wpływ na tempo formowania biofilmu. Metale, takie jak stal ocynkowana czy miedź, wykazują właściwości bakteriostatyczne, jednak z czasem ulegają korozji, tworząc osady sprzyjające adhezji mikroorganizmów. Tworzywa sztuczne (PVC, PEX, PP) charakteryzują się gładką powierzchnią, lecz ich chemiczna obojętność i możliwość uwalniania niewielkich ilości związków organicznych, często przyspieszają rozwój biofilmów. Dodatkowo różnice w ładunku elektrostatycznym i hydrofobowości wpływają na preferencyjne zasiedlanie biofilmu przez określone grupy mikroorganizmów [10].
Nie bez znaczenia pozostaje jakość procesu dezynfekcji czy obecność biocydów. Niskie stężenie środków dezynfekcyjnych, ich nieregularne dawkowanie lub utrata aktywności chemicznej prowadzą do subletalnego stresu, który może paradoksalnie przyspieszyć rozwój biofilmu, poprzez indukcję mechanizmów obronnych i zwiększoną produkcję EPS. Zjawisko to obserwuje się szczególnie w instalacjach z niestabilnym poziomem chloru lub w warunkach nagłych zmian parametrów wody. Jest to zjawisko powiązane ze wzrostem nekrotroficznym, który jest definiowany jako zjawisko polegające na wykorzystywaniu przez bakterie martwych komórek mikroorganizmów jako źródła cennych składników odżywczych [20].
4. Metody ograniczania i usuwania biofilmów
Zintegrowane podejście, które łączy oddziaływanie fizyczne, chemiczne oraz konstrukcyjne jest kluczowym aspektem, pozwalającym na kontrolę i eliminowanie problemów w instalacjach związanych z tworzeniem się biofilmów [6]. Najczęściej podstawę działań prewencyjnych stanowią metody chemiczne, wśród których kluczową rolę odgrywa chlorowanie. Chlor i jego pochodne, zwłaszcza podchloryny, są szeroko stosowane ze względu na dostępność i skuteczność wobec mikroorganizmów. Jednakże ich działanie wobec dojrzałych biofilmów jest ograniczone, ponieważ warstwa EPS utrudnia penetrację środka dezynfekcyjnego do głębszych warstw struktury. Dlatego w celu zwiększenia efektywności dezynfekcji coraz częściej stosuje się dwutlenek chloru. Jest to związek, który wykazuje większą stabilność i skuteczność w szerokim zakresie pH oraz posiada zdolność przenikania przez matrycę biofilmu. Inną grupę stosowanych środków stanowią silne utleniacze, takie jak ozon czy nadtlenek wodoru, które są w stanie degradować polimery pozakomórkowe, prowadząc do naruszenia integralności biofilmu [19].
Równolegle stosuje się metody fizyczne, które pełnią rolę w mechanicznej destabilizacji biofilmów. Płukanie instalacji z wykorzystaniem zwiększonej prędkości przepływu, usuwa luźniejsze warstwy formującego się biofilmu [12]. Z tego względu regularne stosowanie takiego zabiegu uważane jest za kluczowe, w celu zmniejszenia ryzyka dojrzewania biofilmów. W niektórych instalacjach wykorzystuje się także techniki hydrodynamiczne, takie jak czyszczenie rurociągów metodą piggingu. Ta metoda wykorzystuje przesuwanie specjalnych tłoków, usuwających biofilm ze ścian rur. Kolejnym rozwiązaniem jest promieniowanie UV, stosowane głównie w dezynfekcji wody w przepływie. Choć promieniowanie nie usuwa biofilmu z powierzchni rur, skutecznie redukuje ilość mikroorganizmów dostających się do instalacji, ograniczając możliwości rozwoju biofilmu [8]. W ostatnich latach rośnie zainteresowanie wykorzystaniem ultradźwięków, których działanie kawitacyjne może prowadzić do uszkodzenia matrycy EPS i tym samym do rozluźnienia struktury biofilmu [14].
Racjonalne projektowanie instalacji ma decydujący wpływ na ograniczenie adhezji mikroorganizmów, przez stosowanie odpowiednio dobranych rozwiązań materiałowych i konstrukcyjnych. Wybieranie materiałów o mniejszej podatności na kolonizację, takich jak stal kwasoodporna czy odpowiednio modyfikowane tworzywa sztuczne, może znacząco wpłynąć na tempo formowania biofilmów [1]. Coraz częściej w nowo budowanych instalacjach stosuje się powłoki przeciwdrobnoustrojowe, zawierające m.in. jony srebra, miedzi lub wykorzystujące mechanizmy fotokatalityczne, które hamują rozwój mikroorganizmów na powierzchniach kontaktujących się z wodą. Równie ważna jest optymalna konstrukcja, obejmująca eliminację stref stagnacji oraz ograniczenie martwych odcinków. Odpowiednie ukształtowanie systemu przepływu oraz zapewnienie optymalnej prędkości wody, minimalizuje możliwość przylegania komórek bakteryjnych [8].
Dopełnieniem powyższych metod jest równoczesne stosowanie strategii biologicznych, które obecnie znajdują się w fazie intensywnego rozwoju. Jednakże w najbliższym czasie mogą stanowić istotne wsparcie tradycyjnych metod zwalczania biofilmów [2]. Wśród nich największe znaczenie ma zastosowanie endogennych enzymów, degradujących składniki macierzy EPS, takie jak alginianazy czy proteazy, które rozbijają strukturę biofilmu. Coraz szerzej bada się również zastosowanie bakteriofagów. Są to wirusy specyficzne wobec określonych gatunków bakterii, które mogą skutecznie redukować populacje mikroorganizmów, odpowiedzialnych za formowanie biofilmów. Innym podejściem jest stosowanie biokontroli mikrobiologicznej, polegającej na wprowadzaniu niepatogennych szczepów, konkurujących z niepożądanymi bakteriami o przestrzeń i zasoby [20].
5. Podsumowanie
Wyniki prowadzonych badań jednoznacznie wskazują, że żadna pojedyncza metoda nie zapewnia pełnej i długotrwałej eliminacji biofilmów. Skuteczna kontrola wymaga podejścia zintegrowanego. Dostosowane do specyfiki danej instalacji, jej warunków eksploatacyjnych oraz rodzaju występujących mikroorganizmów jest niezbędne do efektywnego ograniczania tworzenia biofilmów. W obliczu rosnących wymagań, dotyczących bezpieczeństwa sanitarnego oraz efektywności systemów wodnych, konieczne jest rozwijanie innowacyjnych technologii, zwłaszcza w obszarze biotechnologii i materiałoznawstwa. Kompleksowe i wieloaspektowe strategie pozostają zatem kluczem do skutecznego ograniczania biofilmów oraz utrzymania wysokiej jakości wody w instalacjach wodociągowych i technicznych [3].
6. Literatura
[1] Stoodley, P., Cargo, R., Rupp, C. J., Wilson, S., & Klapper, I. (2002). Biofilm mechanics and shear-induced deformation and detachment. Journal of Industrial Microbiology and Biotechnology, 29, 361–367. https://doi.org/10.1038/sj.jim.7000282
[2] Wingender, J., & Flemming, H.-C. (2011). Biofilms in drinking water and their role as reservoir for pathogens. International Journal of Hygiene and Environmental Health, 214(6), 417–423. https://doi.org/10.1016/j.ijheh.2011.05.009
[3] World Health Organization. (2022). Drinking-water: Guidelines for drinking-water quality. WHO Press.
[4] Costerton, J. W., Stewart, P. S., & Greenberg, E. P. (1999). Bacterial biofilms: A common cause of persistent infections. Science, 284(5418), 1318–1322. https://doi.org/10.1126/science.284.5418.1318
[5] Ammar, Y., Swailes, D., & Bridgens, B. (2018). Influence of surface roughness on biofilm formation in water distribution systems. Biofouling, 34(2), 179–190.
[6] Beech, I. B., & Sunner, J. (2004). Biocorrosion: Towards understanding interactions between biofilms and metals. Current Opinion in Biotechnology, 15(3), 181–186. https://doi.org/10.1016/j.copbio.2004.05.001
[7] Simões, M., Simões, L. C., & Vieira, M. J. (2010). A review of current and emergent biofilm control strategies. LWT – Food Science and Technology, 43(4), 573–583.
[8] Beneduce, L., et al. (2020). Control strategies of microbial biofilms in water distribution systems. Applied Microbiology and Biotechnology, 104, 7079–7093. https://doi.org/10.1007/s00253-020-10736-4
[9] Flemming, H.-C., & Wingender, J. (2010). The biofilm matrix. Nature Reviews Microbiology, 8, 623–633.
[10] Azeredo, J., Azevedo, N. F., Briandet, R., et al. (2017). Critical review on biofilm methods. Critical Reviews in Microbiology, 43(3), 313–351. https://doi.org/10.1080/1040841X.2016.1208141
[11] Bridier, A., Briandet, R., Thomas, V., & Dubois-Brissonnet, F. (2011). Resistance of bacterial biofilms to disinfectants: A review. Biofouling, 27(9), 1017–1032. https://doi.org/10.1080/08927014.2011.626899
[12] Liu, G., Verberk, J. Q. J. C., & van Dijk, J. C. (2013). Bacterial growth in drinking water distribution systems. Water Research, 47(3), 1075–1087. https://doi.org/10.1016/j.watres.2012.11.042
[13] Donlan, R. M. (2002). Biofilms: Microbial life on surfaces. Emerging Infectious Diseases, 8(9), 881–890.
[14] Lopez, D., Vlamakis, H., & Kolter, R. (2010). Biofilms. Cold Spring Harbor Perspectives in Biology, 2(7), a000398. https://doi.org/10.1101/cshperspect.a000398
[15] Van der Wielen, P. W. J., & van der Kooij, D. (2010). Nontuberculous mycobacteria in drinking water systems: A review. Water Research, 44(15), 4646–4655. https://doi.org/10.1016/j.watres.2010.06.037
[16] Pang, C. M., & Liu, W.-T. (2007). Community structure analysis of reverse osmosis membrane biofilms and the significance of Rhizobiales bacteria in biofouling. Environmental Science & Technology, 41(13), 4728–4734. https://doi.org/10.1021/es0622515
[17] Flemming, H.-C., Wingender, J., Szewzyk, U., et al. (2016). Biofilms: An emergent form of bacterial life. Nature Reviews Microbiology, 14(9), 563–575. https://doi.org/10.1038/nrmicro.2016.94
[18] Hall-Stoodley, L., Costerton, J. W., & Stoodley, P. (2004). Bacterial biofilms: From the natural environment to infectious diseases. Nature Reviews Microbiology, 2(2), 95–108. https://doi.org/10.1038/nrmicro821
[19] Proctor, C. R., & Hammes, F. (2015). Drinking water microbiology—from measurement to management. Current Opinion in Biotechnology, 33, 87–94. https://doi.org/10.1016/j.copbio.2014.12.014
[20] Szewzyk, U., Szewzyk, R., Manz, W., & Schleifer, K.-H. (2000). Microbiological safety of drinking water. Annual Review of Microbiology, 54, 81–127. https://doi.org/10.1146/annurev.micro.54.1.81
[21] Emery Pharma Services. Biofilm formation diagram. Dostęp online: https://www.emerypharmaservices.com/ (dostęp: 6 stycznia 2026).
